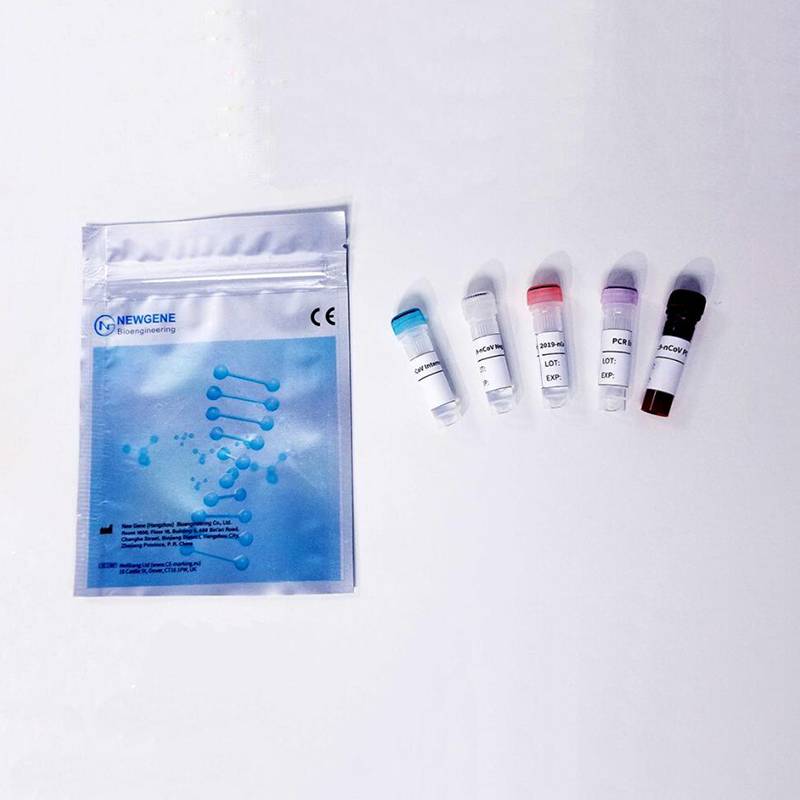
Novel Coronavirus (2019-nCoV) Ribonukleinsäure-Nachweiskit (Echtzeit-PCR – Fluoreszenzsonden-Assay)
BeabsichtigtVerwenden
Dieses Produkt ist für den qualitativen Nachweis des neuartigen Coronavirus (SARS-CoV-2) in Atemwegsproben bestimmt.Die Erkennungsergebnisse können zur Unterstützung der klinischen Diagnose der Coronavirus-Krankheit 2019 (COVID-19) verwendet werden.
Komponenten
2019-nCoV PCR-Puffer – 96 Tests
PCR-Enzymmischung - 96 Tests
2019-nCoV-Positivkontrolle – 48 Tests
2019-nCoV-Negativkontrolle – 48 Tests
2019-nCoV Interne Kontrolle – 96 Tests
Packungsbeilage - 1 Kopie
ProduktMechanismus
Dieses Produkt enthält vier PCR-Primerpaare, vier fluoreszierende Sonden, RNA-Reverse-Transkriptase, DNA-Polymerase, dNTP, Magnesiumionen und andere Chemikalien zum Nachweis viraler RNA.Es zielt gleichzeitig auf das RNA-abhängige RNA-Polymerase (RdRp)-Gen, das Nucleocapsid (N)-Gen und das Envelop (E)-Gen von 2019-nCoV in einem einzigen Reagenzglas ab.Der Testprozess läuft in den folgenden drei Schritten ab: 1) Reverse-Transkription viraler RNA in virale DNA.2) Virale DNA auf eine messbare Menge amplifizieren.3) Geben Sie die Menge an DNA-Amplikons durch Sondenhybridisierung an.Außerdem enthält dieses Produkt auch eine interne Kontrolle und eine externe Kontrolle, um seine Leistung während des Transports und der Lagerung zu überwachen.